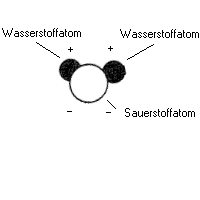
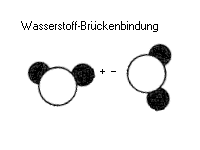
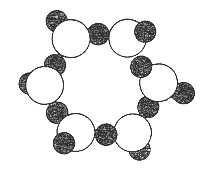
Beim Eis ist schließen sich die Wassermoleküle über die Wasserstoffbrückenbindung zu einem symmetrischen Sechseck zusammen, einem Hexagon
 .
.
Hier kann man schon die symmetrische Struktur der Schneesterne erahnen.
Dieses Hexagon bindet die Moleküle fester als beim Wasser. Die Folge: Es können sich nur wenige Moleküle aus diesen Ketten losreißen und als Wasserdampf in der Luft herumschwirren. Die relative Luftfeuchte muß also über Eis kleiner sein als über Wasser.
Zusammenfassend kann man sagen: Die relative Luftfeuchte ist über Eis kleiner als über einer ebenen Wasserfläche; über dieser ist die Feuchte wiederum kleiner als über einem Tropfen. Diese Feststellung ist wichtig für die Bildung von Wolkentropfen und Niederschlag.